UNIDAD EDUCATIVA HERLINDA TORAL
Tema de la clase: ESTEQUIOMETRIA DE GASES
- Dispositivo/s electrónico/s utilizado/s: PANTALLA INTERACTIVA Y PROYECTOR
- Modelo de interacción: INTERACTIVA 1:1
- Recursos didácticos digitales utilizados: BLOG
- Estrategias pedagógicas aplicadas: DE ANÁLISIS. SÍNTESIS Y VALORACIÓN
- Competencias y habilidades del Siglo XXI desarrolladas: DESARROLLO DE HABILIDADES EN EL MANEJO DE MEDIOS Y TECNOLOGÍAS DE LA INFORMACIÓN.
ESTEQUIOMETRIA
En Química, la estequiometría (del griego στοιχειον, stoicheion, 'elemento' y μετρον, métrón, 'medida') es el cálculo de las relaciones cuantitativas entre los reactivos y productos en el transcurso de una reacción química. Estas relaciones se pueden deducir a partir de la teoría atómica, aunque históricamente se enunciaron sin hacer referencia a la composición de la materia, según distintas leyes y principios.
El primero que enunció los principios de la estequiometría fue Jeremias Benjamin Richter (1762-1807), en 1792, quien describió la estequiometría de la siguiente manera:
«La estequiometría es la ciencia que mide las proporciones cuantitativas o relaciones de masa de los elementos químicos que están implicados (en una reacción química)».
También estudia la proporción de los distintos elementos en un compuesto químico y la composición de mezclas químicas.
John
Dalton diseñó, durante el período
de 1803 a 1807, una teoría atómica con la intención
de dar explicación a varias observaciones
experimentales. Con esta teoría se desechaba
definitivamente la idea de los alquimistas
sobre la transmutación de plomo en oro. Esta
teoría ha perdurado prácticamente intacta
hasta la época actual.
Los
postulados básicos de la Teoría Atómica de Dalton son
los siguientes:
1.Cada
elemento está formado por partículas muy pequeñas
llamadas átomos (en honor de
Demócrito)
2.Todos los
átomos de un mismo elemento son iguales entre sí.
Los átomos de elementos
diferentes son diferentes. Los átomos de elementos
diferentes poseen propiedades
diferentes, incluyendo masas diferentes.
3.Los
átomos de un elemento no pueden ser transformados en
otro tipo de átomos mediante
reacciones químicas. En una reacción química los
átomos no pueden ser creados
ni destruido.
4.Los
compuestos se forman cuando se combinan los átomos de
más de un elemento.
LEYES PONDERALES
La
teoría de Dalton explica varias leyes que ya se
conocían en su época,
denominadas Leyes
Ponderales
Ley de la
composición constante:
En un
compuesto dado los números relativos y las clases de
átomos son iguales. Esta
Ley es la base del postulado de la Ley de la
conservación de la masa o Ley de la conservación
de la materia:
La masa
total de los
materiales presentes después de una reacción química
es la misma que la masa total antes de
la reacción. Esta ley
es la base del postulado de la Ley de
las proporciones múltiples:
si dos
elementos A y B se combinan para formar más de un
compuesto, las masas de B que se pueden combinan con
una masa dada de A están en proporciones de números enteros sencillos.

Estas leyes ponderales de la Estequiometria pueden resumirse en el siguiente video; con lo cual podemos comprender de mejor manera estos enunciados:
- La densidad de un gas es de 2,37 g/L a 25 °C Y 873 torr. Calcula el peso molecular del gas.
- Indica en cuánto aumenta la masa de 3,55 g de sulfato de sodio al convertirse completamente en sulfato de sodio decahidratado.
- Un mol de gas a 50 ºC y 2 atm de presión tiene una densidad de 3,5 mg/mL . Determinar cuál es la masa molecular del gas.
- Se coloca un gas ideal en un recipiente cerrado. Cuando la temperatura aumenta en 10º, la presión aumenta un 2
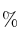 . Indica la temperatura inicial expresada en escala Celsius.
. Indica la temperatura inicial expresada en escala Celsius.
"COMPARTE CON TUS AMIGOS LO APRENDIDO EN CLASES, RECUERDA QUE ES IMPORTANTE TENER MAS DE UNA OPINION DE LO ESTUDIADO"
ING. QUIMICO JUAN URDIALES FLORESDOCENTE FISICO-QUIMICA
UNIDAD EDUCATIVA HERLINDA TORAL

No hay comentarios:
Publicar un comentario